Nhôm
- Nhôm bắt nguồn từ tiếng Pháp: aluminium, ký hiệu: Al.
- Nhôm là nguyên tố phổ biến sau oxi và silic, và là kim loại phổ biến nhất trong vỏ Trái Đất.


Vị trí trong bảng tuần hoàn, cấu hình electron nguyên tử
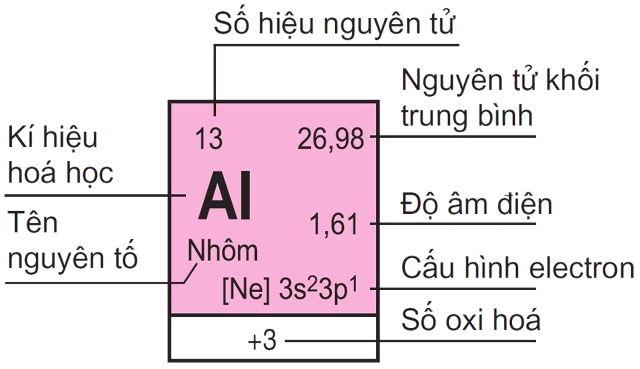
- Nhôm có số nguyên tử là 13. Nguyên tử khối là 27u.
- Cấu hình electron nguyên tử: \( 1s^{2}2s^{2}2p^{6}3s^{2}3p^{1} \).
- Nhôm dễ nhường cả 3 electron hóa trị nên có số oxi hóa +3 trong các hợp chất.

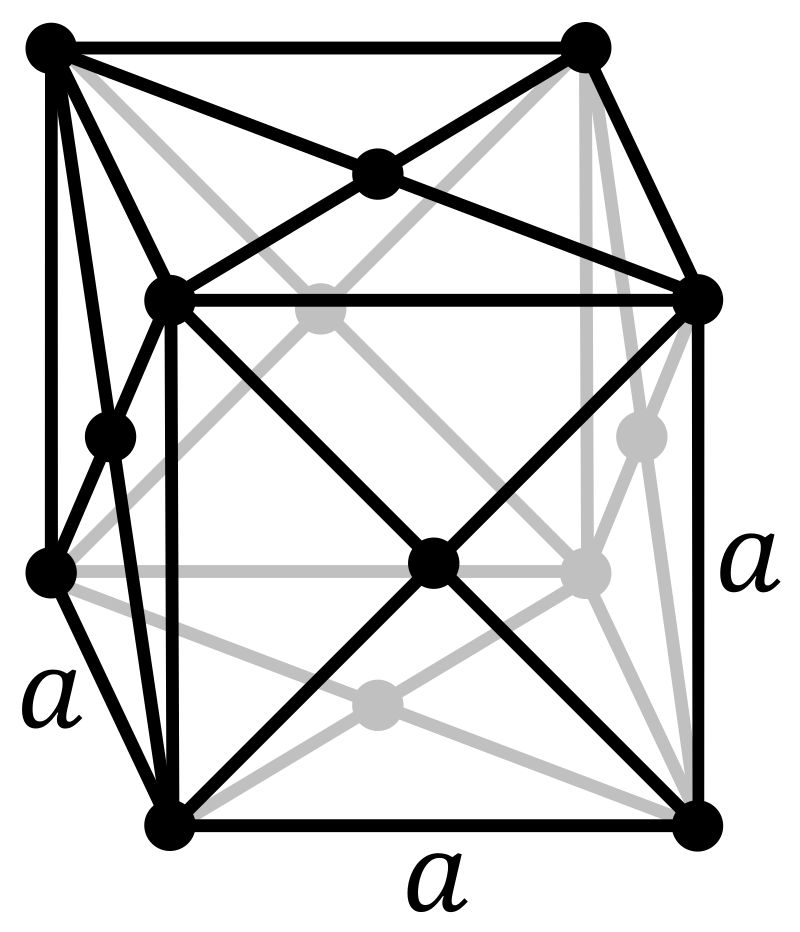
Tính chất vật lý

Tính chất hóa học
Tính khử mạnh, chỉ sau kim loại kiềm và kiềm thổ, nên dễ bị oxi hóa thành ion dương:
\( Al \rightarrow Al^{3+} + 3e \)
Tác dụng với phi kim
Khử dễ dàng các nguyên tử thành ion âm.
Tác dụng với halogen
Bột nhôm tự bốc cháy khi tiếp xúc với khí clo:
\( 2Al + 3Cl_{2} \rightarrow 2AlCl_{3} \)
Tác dụng với Oxi
Khi đốt, bột nhôm cháy trong không khí với ngọn lửa sáng chói, tỏa nhiều nhiệt, tạo ra chất rắn màu trắng nhôm oxit (Al2O3):
\( 4Al + 3O_{2} \overset{t^{o}}{\rightarrow} 2Al_{2}O_{3} \)
Tác dụng với axit
- Nhôm khử dễ dàng ion H+ trong dung dịch HCl và H2SO4 loãng tạo thành khí H2:
\( 2Al + 6HCl \rightarrow 2AlCl_{3} + 3H_{2} \) - Nhôm tác dụng mạnh với dung dịch HNO3 loãng, HNO3 đặc, nóng và H2SO4 đặc, nóng:
\( Al+4HNO_{3}\left ( loãng \right )\overset{t^{o}}{\rightarrow} Al(NO_{3})_{3}+ NO +2H_{2}O \) \( 2Al + 6H_{2}SO_{4} \overset{t^{o}}{\rightarrow} Al_{2}(SO_{4})_{3} + 3SO_{2} + 6H_{2}O \) - Thụ động bởi dung dịch axit HNO3 đặc, nguội hoặc H2SO4 đặc, nguội.
Tác dụng với oxit kim loại
- Phản ứng nhiệt nhôm là phản ứng hóa học tỏa nhiệt trong đó nhôm là chất khử ở nhiệt độ cao. Ví dụ nổi bật nhất là phản ứng nhiệt nhôm giữa oxit sắt (III) và nhôm:
\( 2Al + Fe_{2}O_{3}\overset{t^{o}}{\rightarrow} Al_{2}O_{3} + 2Fe \) - Ứng dụng: điều chế lượng nhỏ sắt nóng chảy khi hàn đường ray.
Tác dụng với nước
-
Al không phản ứng với nước vì được lớp oxit mỏng, bền và đặc khít bảo vệ.
-
Nếu phá bỏ lớp oxit bao phủ bề mặt, Al phản ứng trực tiếp với nước ở nhiệt độ thường tạo thành chất kết tủa dạng keo trắng
\( 2Al + 6H_{2}O \rightarrow 2Al(OH)_{3} + 3H_{2} \)
Tác dụng với dung dịch kiềm
- Nhôm oxit là oxit lưỡng tính nên lớp màng mỏng Al2O3 trên bề mặt nhôm tác dụng với dung dịch kiềm tạo ra muối tan.
\( Al_{2}O_{3} + 2NaOH \rightarrow NaAlO_{2} + H_{2}O \) - Khi không còn màng oxit bảo vệ, nhôm tác dụng với nước tạo ra Al(OH)3 và giải phóng khí H2:
\( 2Al + 6H_{2}O \rightarrow 2Al(OH)_{3} + 3H_{2} \) - Al(OH)3là hidroxit lưỡng tính nên tác dụng tiếp với dung dịch kiềm:
\( Al(OH)_{3}+NaOH \rightarrow NaAlO_{2}+2H_{2}O \) - Từ quá trình trên, ta có phương trình hóa học sau:
\( 2Al + 2NaOH + 2H_{2}O\rightarrow 2NaAlO_{2}+3H_{2} \)
Ứng dụng và trạng thái tự nhiên
Ứng dụng
Trạng thái tự nhiên
- Nhôm là kim loại thường thấy trong vỏ Trái Đất (chiếm khoảng 8%)
- Nhôm là kim loại hoạt động mạnh nên trong tự nhiên chỉ tồn tại ở dạng hợp chất.
- Trong tự nhiên, nhôm thường có trong các hợp chất như đất sét, boxit hay criolit. Cụ thể:
- Trong đất sét: Al2O3.2SiO2.2H2O
- Trong mica: K2O.Al2O3.6SiO2
- Trong boxit: Al2O3.2H2O
- Trong criolit: 3NaF.AlF3
Sản xuất nhôm
- Nguyên liệu: Quặng boxit Al2O3.2H2O.
- Trong công nghiệp, nhôm được sản xuất bằng phương pháp điện phân nhôm oxit nóng chảy, xúc tác criolit (CTPT là Na3AlF6 hay 3NaF.AlF3):
\( 2Al_{2}O_{3} \xrightarrow[dpnc]{criolit} 4Al + 3O_{2} \)
Điện phân nhôm oxit nóng chảy
Một số hợp chất quan trọng của nhôm
Nhôm Oxit
Tính chất
- Oxit nhôm hay nhôm oxit, còn gọi là alumine là một hợp chất hóa học của nhôm và oxi với công thức hóa học Al2O3.
- Là chất rắn màu trắng, không tan trong nước và không tác dụng với nước, nóng chảy trên 2050oC.
- Oxit nhôm là thành phần chính của Boxit, loại quặng chủ yếu chứa nhôm.
- Oxit nhôm là một oxit lưỡng tính nên vừa tác dụng với axit, vừa tác dụng với dung dịch kiềm như:
\( Al_{2}O_{3} + 2NaOH \rightarrow NaAlO_{2} + H_{2}O \) \( Al_{2}O_{3}+6HCl\rightarrow 2AlCl_{3} + 3H_{2}O \)
Ứng dụng
Nhôm Hydroxit
- Là chất rắn màu trắng, kết tủa ở dạng keo.
- Là hydroxit lưỡng tính.
- Nhôm hydroxit có tính bazo trội hơn tính axit. Do có tính axit nên còn có tên là axit aluminic, là axit rất yếu, yếu hơn axit cacbonic.
Nhôm Sunfat
- Muối nhôm sunfat khan tan trong nước tỏa nhiệt làm dung dịch nóng lên do bị hydrat hóa.
- Muối nhôm sunfat có nhiều ứng dụng nhất là muối sunfat kép của nhôm và kali ngậm nước gọi là phèn chua: K2SO4.Al2(SO4)3.24H2O








No Comments
Leave a comment Cancel